前列腺癌是男性生殖系统最常见的恶性肿瘤之一,在我国的发病率逐年升高。由于早期前列腺癌缺乏特异性症状,易与良性前列腺增生相混淆,待临床出现血尿、尿潴留等症状时,肿瘤往往进展至中晚期。因此早期诊断对于前列腺癌的治疗时机把握、方案选择都至关重要[1]。
为了推进我国前列腺癌筛查服务的规范化、优质化和均质化,为筛查相关工作人员提供科学的、可操作性强的前列腺癌筛查指导,国内专家学者制定了《中国前列腺癌筛查与早诊早治指南(2022,北京)》(以下简称《指南》)[2]。下面将详细解读该《指南》的前半部分,即中国前列腺癌的流行病学情况、疾病分型、风险人群和早筛建议。
我国前列腺癌疾病负担较重,2015年全国前列腺癌发病例数约7.2万,占男性全部恶性肿瘤新增病例的3.35%,城市地区前列腺癌发病率高于农村地区[3]。研究显示,与1990年相比,2013年我国男性前列腺癌发病人数、死亡人数、标化发病率及标化死亡率均大幅增加,发病人数从1.38万增至8.14万,增加490.27%;死亡人数从0.58万增至1.78万,增加206.86%;标化发病率由4.48/10万增至13.33/10万,增加197.54%;标化死亡率也由2.26/10万增至3.32/10万,增加46.9% [4]。而且我国前列腺癌患者5年生存率与欧美等发达国家和地区存在差距[2]。
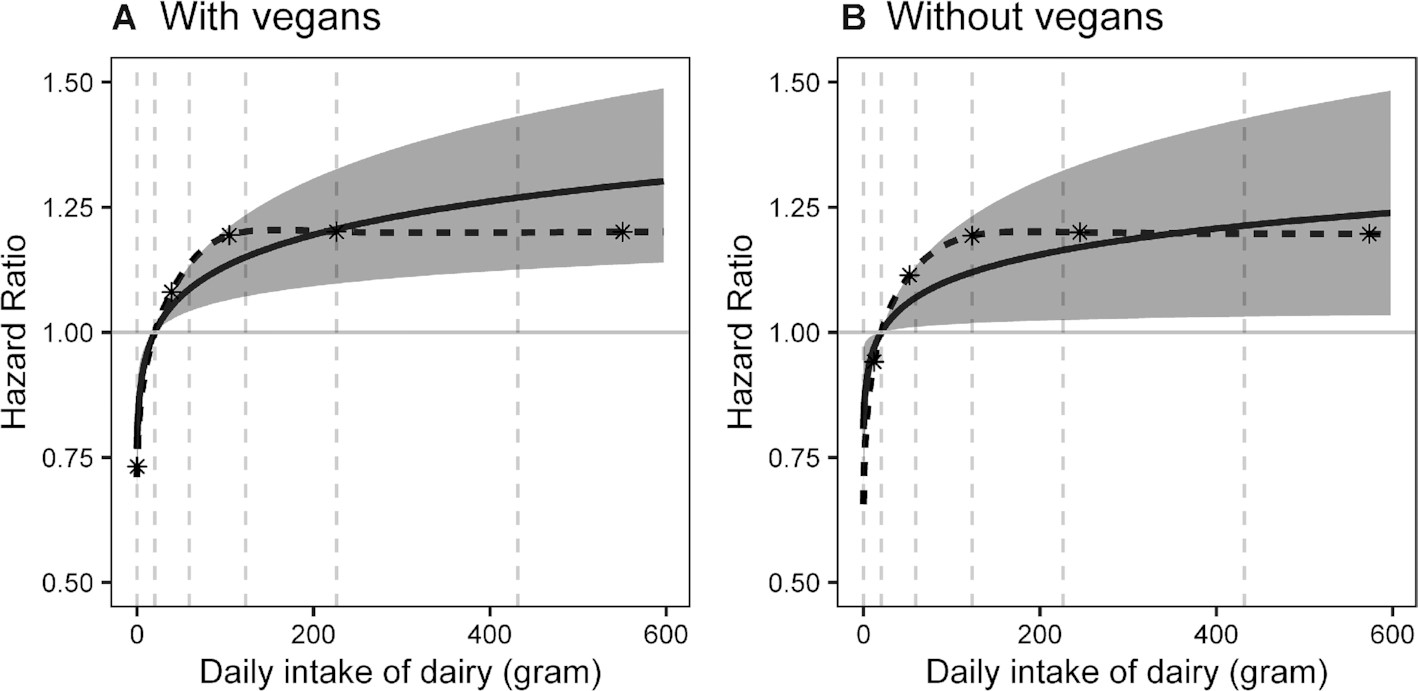
前列腺癌相关危险因素包括:年龄、前列腺癌家族史和乳腺癌家族史、吸烟、肥胖、前列腺炎、良性前列腺增生、过多摄入牛奶或相关乳制品、钙、锌。摄入绿茶、大豆类食品可能降低前列腺癌发生风险[2]。
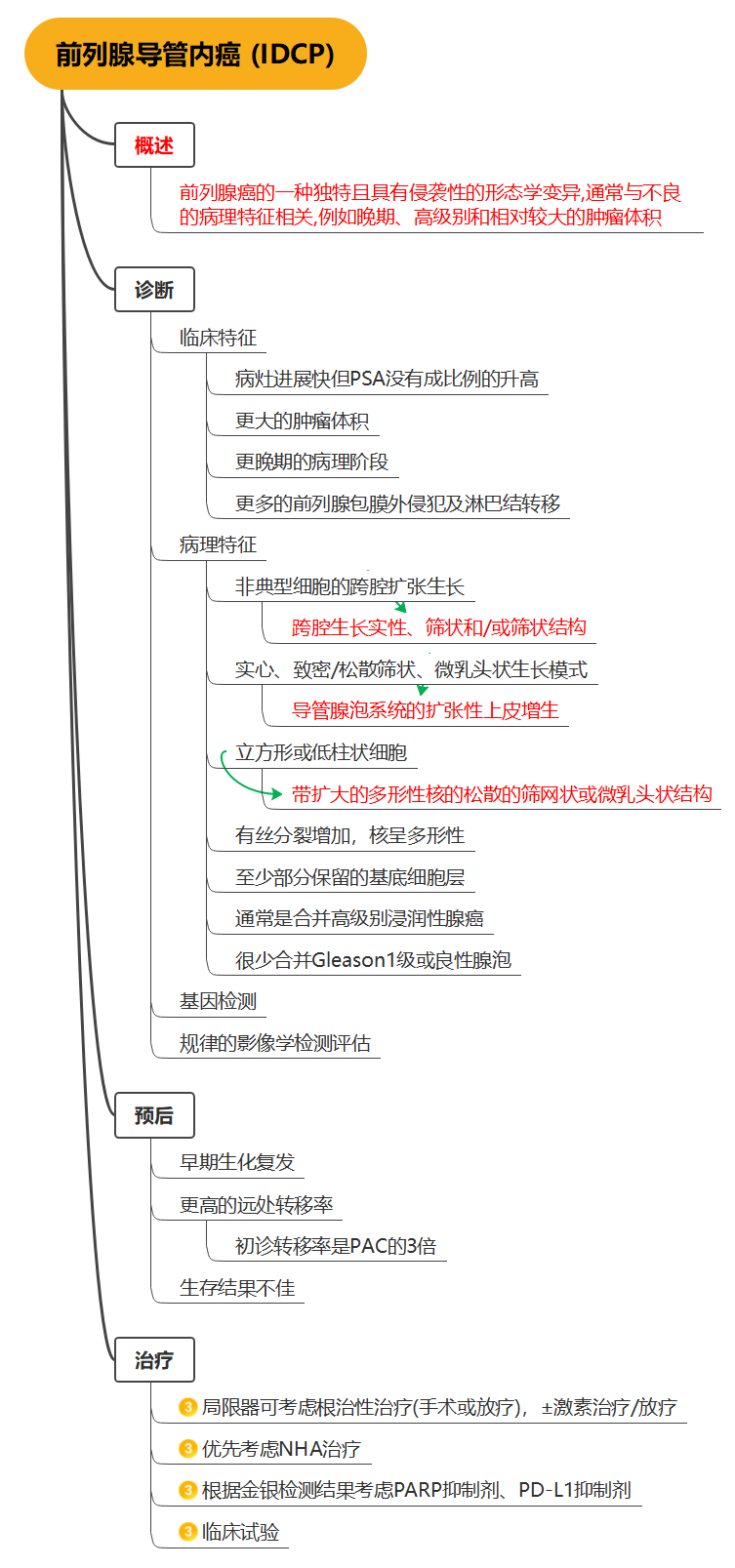
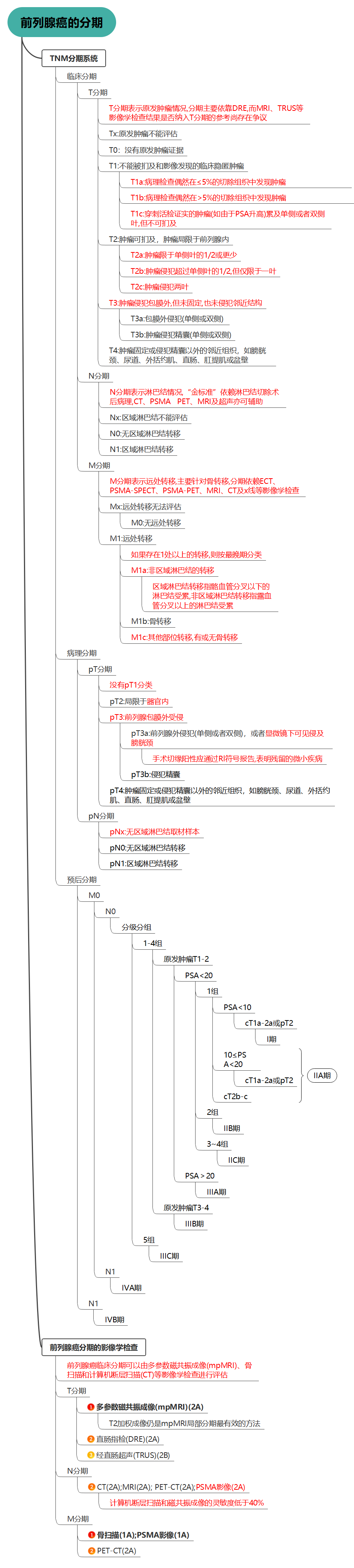
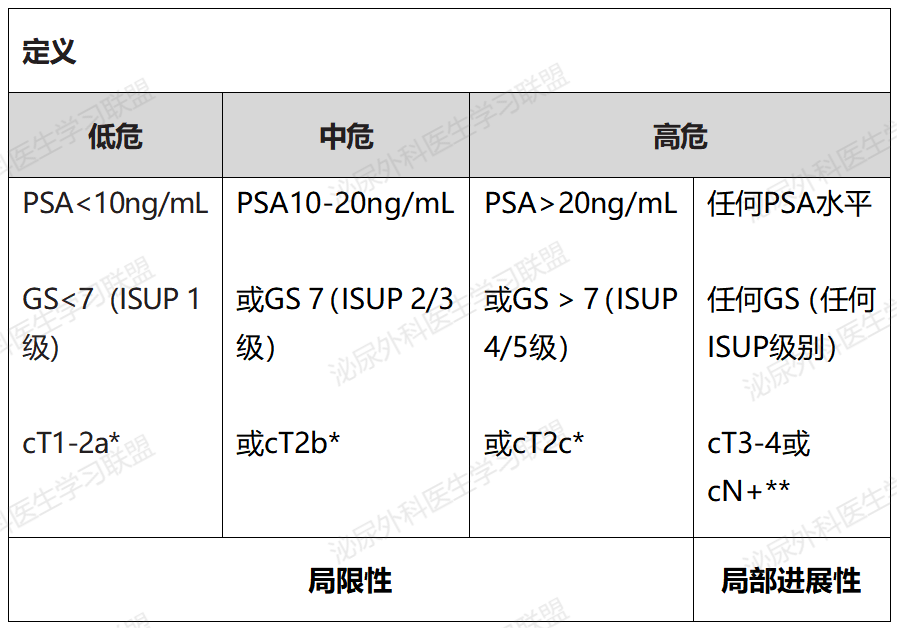
前列腺癌病理类型包括腺泡腺癌、导管内癌、导管腺癌、尿路上皮癌、鳞状细胞癌、基底细胞癌和神经内分泌肿瘤等,目前应用最广泛的分级方法是Gleason评分系统,将前列腺癌组织分为主要形态分级区和次要形态分级区,根据Gleason总评分和疾病危险度的不同可将前列腺癌分为5个不同的组别。《指南》推荐采用美国癌症联合委员会第8版TNM分期系统,将前列腺癌预后分组为Ⅰ期、Ⅱ期、Ⅲ期和Ⅳ期,美国癌症联合委员会前列腺癌TNM分期和预后分组对应表如下表所示[2]。
表1. 美国癌症联合委员会前列腺癌TNM分期和预后分组对应表
前列腺癌筛查的潜在负面效应主要有4个方面:筛查假阳性、过度诊断、过度治疗、相关心理影响[2]。
-
筛查假阳性:基于前列腺特异抗原(PSA)检测开展的前列腺癌筛查可能引起筛查假阳性,一项欧洲前列腺癌筛查随机研究的假阳性筛查结果显示,≥70岁男性的假阳性率为20.6%,65-69岁男性的假阳性率为14.5%,60-64岁男性的假阳性率为11.1%,55-59岁男性的假阳性率为6.4%,<55岁男性的假阳性率为3.5% [5]。
-
过度诊断:德国卫生保健质量和效率研究所收集11项随机对照试验,分析结果显示,基于PSA检测的前列腺癌筛查随机对照研究中报告的过度诊断率为0.7%-6.0%[6]。
-
过度治疗:过度诊断经常伴随着过度治疗,由于前列腺靠近膀胱、阴茎和直肠,治疗常导致出现长期的泌尿系统、生殖系统和肠道症状[7]。
-
相关心理影响:筛查可能导致对不严重的前列腺癌进行过度检测和治疗,其结果是医疗费用增加,不良反应和并发症的增多,加重患者的焦虑情绪。PSA检测的特异性和敏感性均不高,假阳性结果会导致患者焦虑,增加不必要的诊断性操作[8]。
《指南》指出预期寿命10年以上且符合下列条件之一的男性为前列腺癌高风险人群[2]:
上述高风险人群以外的所有男性为一般风险人群,该《指南》推荐详细告知45岁及以上有前列腺癌家族史的男性人群关于筛查的已知和潜在危害及获益,随后可结合专科医师建议决定是否进行前列腺癌筛查 [2]。
《前列腺癌筛查中国专家共识(2021年版)》指出,对于需要进行前列腺癌筛查的人群,应当每2年进行1次血清PSA检测,当受试者PSA<4 μg/L时,建议进行每2年1次的随访;当受试者PSA≥4 μg/L时,应及时通知到受试者本人或家属,并建议受试者转诊至医院进行进一步诊断、治疗和随访[9]。
该《指南》考虑到中国人群基数大而医疗卫生资源相对紧张的现况,以及前列腺癌筛查在各级医疗卫生机构的可操作性,指出已接受筛查且预期寿命10年以上的男性,推荐每2年检测1次血清PSA[2]。
关于筛查停止时间,加拿大泌尿外科协会建议停止前列腺癌筛查的年龄应该基于PSA基线水平和预期寿命:60岁且PSA<1.0 ng/mL的男性,考虑停止PSA筛查;预期寿命<10年的男性,停止PSA筛查[10]。该《指南》综合国际相关指南,推荐PSA检测水平<1.0 ng/mL的60岁及以上男性停止筛查,推荐预期寿命<10年者停止筛查[2]。该《指南》结合我国前列腺癌筛查实践和70岁以上年龄组发病水平高的情况,推荐年龄≥75岁的男性结合个人健康状况选择是否停止筛查[2]。
随着中国经济水平提高、人民生活水平改善和人均寿命延长,中国前列腺癌的发病率呈显著上升趋势,正逐步成为影响中国中老年男性健康的重要疾病。2015年中国前列腺癌的总体发病率为10.23/10万人,死亡率为4.36/10万人。据世界卫生组织国际癌症研究机构统计预测,2020年中国前列腺癌发病率约15.6/10万人,新发病例超11万人,死亡人数超5万人[1]。
和其他癌症不同,前列腺癌患者在早期几乎没有任何症状,这导致前列腺癌容易被忽视,公众早期筛查意识薄弱。在我国,超过2/3的前列腺癌患者初诊时已属中晚期或局部晚期,错过了最佳治疗机会,“早筛、早诊、早治”是提高患者5年生存率行之有效的方法之一 [2]。前列腺癌高风险人群筛查与患者的早诊早治对提高前列腺癌治愈率至关重要,为了促进中国前列腺癌筛查的同质性和规范性,提高前列腺癌筛查的效果,国内专家学者制定了《中国前列腺癌筛查与早诊早治指南(2022,北京)》(以下简称《指南》)[3]。下面将详细解读该《指南》的后半部分,即中国前列腺癌的筛查手段建议、筛查组织流程与随访建议。
前列腺癌筛查应采取何种技术手段ZGX帝国网站管理系统
前列腺特异抗原(PSA)及游离前列腺特异抗原( f-PSA) 明显升高,可以作为前列腺癌早期诊断的参考。过去几年,由于PSA筛查具有特异性强、灵敏度高,检测准确的优点,可作为人群筛查指标[4]。该《指南》推荐首选PSA作为前列腺癌筛查手段[3]。
美国PLCO试验设定PSA检测水平临界值为4.0ng/mL[5],还有一项Meta分析评价了PSA在中国人群前列腺癌早期筛查中的价值,以4.0ng/mL作为临界点检测前列腺癌的灵敏度、特异度和集成受试者工作特征曲线的曲线下面积,分别为91%、41%和0.91[6]。结合上述证据,该《指南》建议在我国的前列腺癌筛查中,PSA临界值设定为4.0 ng/mL[3]。
关于其他筛查手段,2015年国家卫生和计划生育委员会发布的《前列腺特异性抗原检测前列腺癌临床应用》指出,血清PSA浓度≥4.0μg/L时,应配合做直肠指检(DRE)检查,若DRE阳性,则应进一步做前列腺穿刺活组织检查,以明确诊断。若DRE阴性,宜进行f-PSA百分比检测。若f-PSA百分比检测结果<10%,则应考虑进行前列腺穿刺活组织检查,以明确诊断[7]。
该《指南》推荐DRE在PSA初检阳性时作为辅助检查,不推荐单独使用DRE进行前列腺癌筛查,不推荐单独使用正电子发射计算机断层扫描(PET-CT)、 超声或磁共振成像进行前列腺癌筛查[3]。对于前列腺特异性抗原前体 (p2PSA)和前列腺健康指数(PHI),《前列腺癌筛查中国专家共识(2021年版)》明确不推荐将p2PSA、PHI等作为前列腺癌筛查的常规手段[1],该《指南》也不推荐将p2PSA、p2PSA百分比、PHI作为前列腺癌筛查的常规手段 [3]。
解读前列腺癌筛查组织流程与随访ZGX帝国网站管理系统
血PSA检测作为筛查前列腺癌的手段被广泛应用于临床,然而目前利用血清PSA检测为技术手段的前列腺癌筛查仍存在较大争议,并伴随着过度诊断和过度治疗的问题,《指南》不建议对前列腺癌开展无选择性大规模组织性筛查。基于我国人群中高侵袭性和晚期前列腺癌占比较高,《指南》建议高风险人群在充分知晓筛查获益和危害后,与专科医师共同决定是否进行前列腺癌筛查[3]。
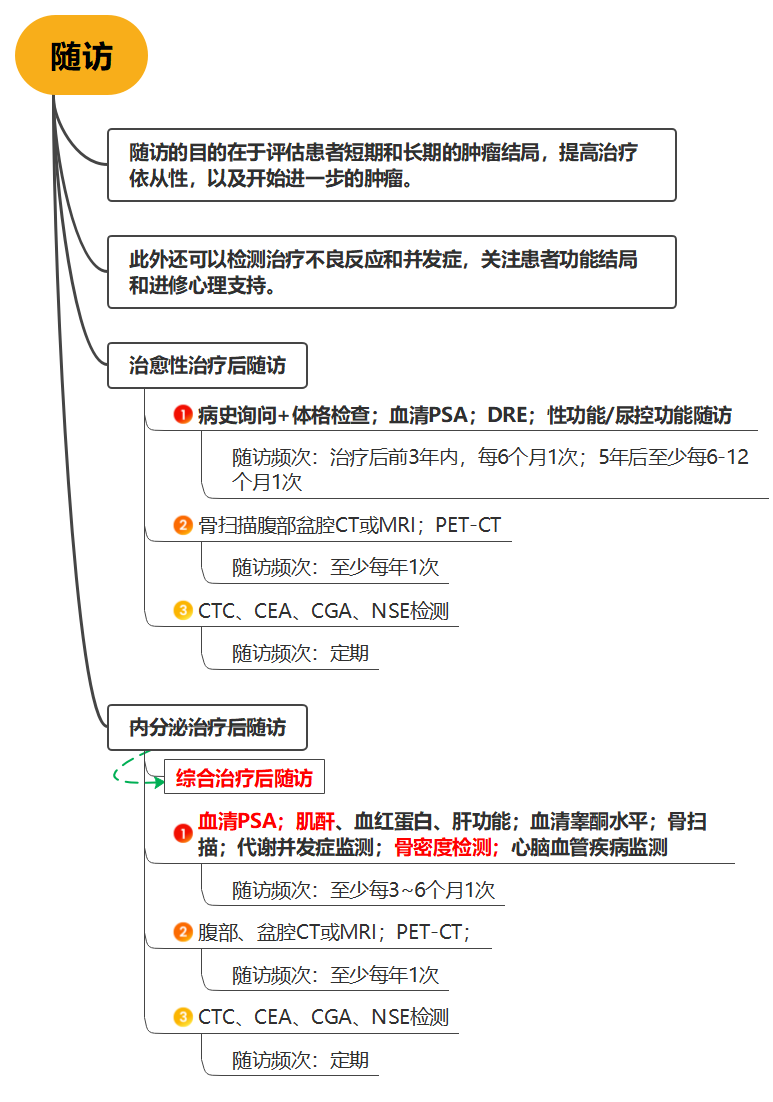
前列腺癌筛查流程主要包括确定前列腺癌高风险人群、充分知情同意、血清PSA检测、结果管理和随访,如图1所示[3]。
知情同意权是病人的一项基本权利。医院在工作中为充分保障病人的知情同意权,减少不必要的纠纷,制作了各种知情同意书,作为与患者及其家属履行知情同意谈话的记录被保存下来[8]。该《指南》在保护医患双方的原则下,推荐前列腺癌筛查前必须签署知情同意书。知情同意书中至少且必须包括:筛查的目的与意义、筛查可获得的益处及不可避免的风险、筛查方式与费用、自愿与保密原则、筛查者或委托人签字和签署日期[3]。
关于随访,《大型人群队列终点事件长期随访技术规范》指出,承担随访工作的业务人员应定期开展集中培训,培训的核心内容包括随访时间、内容、方法(流程)、质控要求及评价指标等[9]。因此,《指南》建议由初检医师或已接受随访技术培训的医务人员对筛查、随访和复查结果进行跟踪[3]。
关于筛查结果管理,《前列腺癌诊疗规范(2018 年版)》指出血清总PSA>4.0ng/mL为异常,初次PSA异常者需要复查[10]。该《指南》表示,如果两次血清PSA>4.0 ng/mL,排除影响 PSA检测水平其他因素干扰后,推荐由泌尿专科医师引导进一步临床检查和干预;如果血清 PSA≤4.0 ng/mL,建议定期监测血清PSA水平[3]。
在质量控制方面,检验质量是直接反映临床检验工作的重要指标之一,加强临床检验的质量控制、提升临床检验管理质量是管理者亟待解决的问题[11]。该《指南》推荐负责风险评估人员应接受专业培训后上岗,筛查需在具有恶性肿瘤筛查资质和PSA检测能力的医疗机构中进行。血液标本按照相关规定进行保存,在PSA检测过程中,建议注意排除多种因素对检测结果的影响,在PSA连续检测时建议在同一检测系统中进行,以保证测定结果的可比性[3]。
该《指南》针对前列腺癌筛查技术、流程、质量控制等多个关键问题给出了详细的循证推荐,可应用于指导中国前列腺癌筛查实践,提高我国前列腺癌筛查同质化和优质化,提升人群筛查获益,以期降低我国前列腺癌死亡率。
[1] 中国抗癌协会泌尿男生殖系统肿瘤专业委员会前列腺癌学组.前列腺癌筛查中国专家共识(2021年版)[J].中国癌症杂志,2021,31(5):435-440.
[2] 邢念增.每年一次PSA筛查,揪出“男性隐藏杀手”[J].人人健康,2021(13):30.
[3] 赫捷,陈万青,李霓,曹巍,叶定伟,马建辉,邢念增,彭绩,田金徽,中国前列腺癌筛查与早诊早治指南制定专家组,中国前列腺癌筛查与早诊早治指南制定工作组.中国前列腺癌筛查与早诊早治指南(2022,北京)[J].中华肿瘤杂志,2022,44(1):29-53.
[4]张卫平,戴继舫.前列腺癌PSA筛查:基于流行病学的证据[J].公共卫生与预防医学,2014,25(06):74-76.
[5]Andriole GL, Crawford ED, Grubb RL 3rd, et al. Mortality results from a randomized prostate-cancer screening trial. N Engl J Med. 2009;360(13):1310-1319.
[6]王宝华,沙宇婷,何凤蝶,吴静.前列腺特异性抗原对中国人群前列腺癌早期 检测价值的Meta分析[J].中国癌症杂志,2020,30(11):879-886.
[7]吴健民,杨振华,马嵘等.前列腺特异性抗原检测前列腺癌临床应用 WS/T 460-2015[S]. 北京:中华人民共和国卫生和计划生育委员会 ,2015.
[8]柴家财,王亮,杜守业.正确认识知情同意书[J].中国病案,2005,6(3):22-23.
[9]中华预防医学会.大型人群队列终点事件长期随访技术规范(T/CPMA 002-2019)[J].中华流行病学杂志,2019,40(7):748-752.
[10]中华人民共和国国家卫生健康委员会. 前列腺癌诊疗规范(2018 年版)[EB/OL].
[11]杨祥康,陈静,魏宇峰,毛亚飞.临床检验影响因素及质量控制分析[J].中医药管理杂志,2020,28(6):63-65.